De fascinerende wereld van atoomstralen in d-blok elementen
Ooit afgevraagd hoe de grootte van een atoom de eigenschappen van een element beïnvloedt? Welkom in de fascinerende wereld van atoomstralen, met name binnen de d-blok elementen. Deze elementen, gelegen in het hart van het periodiek systeem, vertonen unieke trends in hun atoomgrootte die een sleutelrol spelen in hun chemisch gedrag. Van de glinsterende glans van goud tot de magnetische aantrekkingskracht van ijzer, de atoomstraal is een onmisbare factor in het begrijpen van deze veelzijdige elementen.
De atoomstraal, simpel gezegd, is de afstand van de kern van een atoom tot de buitenste elektronenschil. Binnen de d-blok elementen is de trend in atoomstralen niet zo rechtlijnig als in andere groepen. Verschillende factoren spelen een rol, zoals de toenemende nucleaire lading, de afscherming door innerlijke elektronen en de elektron-elektron afstoting. Het ontrafelen van deze invloeden is cruciaal voor het voorspellen en verklaren van de chemische reactiviteit en fysische eigenschappen van d-blok elementen.
Historisch gezien is het bepalen van atoomstralen een uitdaging geweest. Vroege methoden waren gebaseerd op kristallografische gegevens en benaderingen. Met de ontwikkeling van geavanceerde technieken, zoals röntgendiffractie, is het mogelijk geworden om nauwkeurigere metingen te verrichten. Het begrijpen van atoomstralen heeft bijgedragen aan de ontwikkeling van nieuwe materialen, katalysatoren en technologische toepassingen.
Het belang van atoomstralen reikt verder dan de academische wereld. Kennis van atoomstralen is essentieel voor het begrijpen van chemische binding, de vorming van moleculen en de interactie tussen atomen. In de materiaalkunde speelt de atoomstraal een cruciale rol bij het ontwerpen van nieuwe legeringen en materialen met specifieke eigenschappen.
Een van de belangrijkste problemen met betrekking tot atoomstralen binnen de d-blok elementen is de zogenaamde 'lanthanidecontractie'. Dit fenomeen beschrijft de afname in atoomstraal van de lanthaniden, die invloed heeft op de atoomstralen van de elementen die na hen komen in het periodiek systeem. Dit effect is te wijten aan de slechte afscherming van de 4f-elektronen, waardoor de effectieve nucleaire lading toeneemt en de atoomstraal kleiner wordt.
De atoomstraal van een element is geen vaste waarde, maar kan variëren afhankelijk van de oxidatietoestand en de chemische omgeving. Zo kan de atoomstraal van ijzer variëren afhankelijk van of het zich in de Fe2+ of Fe3+ toestand bevindt.
Voor- en nadelen van kennis over atoomstralen in d-blok elementen
| Voordelen | Nadelen |
|---|---|
| Begrijpen van chemische reactiviteit | Complexiteit van trends binnen de d-blok |
| Ontwerpen van nieuwe materialen | Invloed van meerdere factoren op atoomstraal |
Veelgestelde vragen:
1. Wat is een atoomstraal? Antwoord: De afstand van de kern tot de buitenste elektronenschil.
2. Waarom zijn atoomstralen belangrijk? Antwoord: Ze beïnvloeden chemische en fysische eigenschappen.
3. Wat is de lanthanidecontractie? Antwoord: De afname in atoomstraal van de lanthaniden.
4. Hoe worden atoomstralen gemeten? Antwoord: Met behulp van technieken zoals röntgendiffractie.
5. Hoe beïnvloedt de oxidatietoestand de atoomstraal? Antwoord: Hogere oxidatietoestanden leiden tot kleinere atoomstralen.
6. Wat is de relatie tussen atoomstraal en chemische binding? Antwoord: De atoomstraal beïnvloedt de bindingslengte en -sterkte.
7. Welke rol spelen atoomstralen in materiaalkunde? Antwoord: Ze beïnvloeden de eigenschappen van legeringen en materialen.
8. Wat zijn de trends in atoomstralen binnen de d-blok elementen? Antwoord: Complex en beïnvloed door meerdere factoren.
Tips en trucs: Bestudeer de trends in het periodiek systeem en overweeg de invloed van de lanthanidecontractie.
Conclusie: Atoomstralen spelen een cruciale rol in de chemie van d-blok elementen. Begrijpen van de trends en invloeden op atoomstralen is essentieel voor het voorspellen van chemisch gedrag, het ontwerpen van nieuwe materialen en het bevorderen van technologische vooruitgang. Verder onderzoek naar atoomstralen zal leiden tot een dieper begrip van de complexe wereld van de chemie en materiaalkunde. Duik dieper in deze fascinerende wereld en ontdek de geheimen die schuilgaan achter de atoomstraal. De kennis van atoomstralen opent deuren naar nieuwe mogelijkheden in diverse wetenschappelijke disciplines en draagt bij aan de ontwikkeling van innovatieve oplossingen voor wereldwijde uitdagingen.
.png)
Smallest Atomic Radius On Periodic Table at Juan McNair blog | YonathAn-Avis Hai

atomic radii of d block elements | YonathAn-Avis Hai

Atomic Radius and Ionic Radius | YonathAn-Avis Hai

atomic radii of d block elements | YonathAn-Avis Hai

Ionic radius of Period 3 Elements | YonathAn-Avis Hai

Printable Periodic Table With Oxidation Numbers | YonathAn-Avis Hai

The Transition Elements d | YonathAn-Avis Hai

WebElements Periodic Table Periodicity Atomic radii Clementi d | YonathAn-Avis Hai
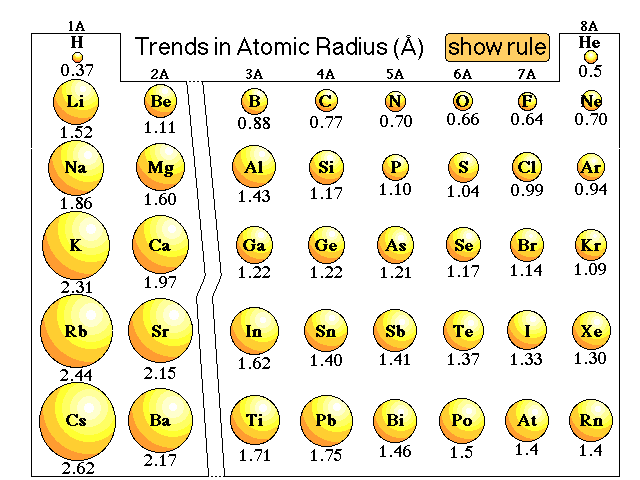
atomic radii of d block elements | YonathAn-Avis Hai

What Does Ne Mean On The Periodic Table at Casey Messenger blog | YonathAn-Avis Hai

d and f Block Elements | YonathAn-Avis Hai

Share 68 kuva d block s te fan twilight zone | YonathAn-Avis Hai

atomic radii of d block elements | YonathAn-Avis Hai

Electron Configuration Periodic Table Elements Chemistry 49 OFF | YonathAn-Avis Hai

The ionic radius of helium is 93 | YonathAn-Avis Hai